研究背景
恶性黑色素瘤是皮肤癌中蕞致命的类型。虽然它在所有皮肤癌中占比不到 5%,却导致了约 72% 的皮肤癌相关死亡。早期黑色素瘤患者通过手术切除,5 年相对生存率可达 99%;但晚期或转移性患者,生存率会大幅下降,区域转移性患者 5 年生存率为 68%,远处转移性患者仅 30%。目前,早期诊断黑色素瘤面临诸多挑战,传统诊断方法如视觉检查和触诊依赖医生经验,现有成像辅助手段,如反射共聚焦显微镜、光学相干断层扫描等,存在设备昂贵、有辐射等问题。近红外荧光成像虽有应用,但常用的吲哚菁绿(ICG)存在非特异性积累、激光穿透浅、光漂白快等缺点,导致假阳性率高、体内半衰期短。因此,开发更精准有效的黑色素瘤早期诊断方法迫在眉睫。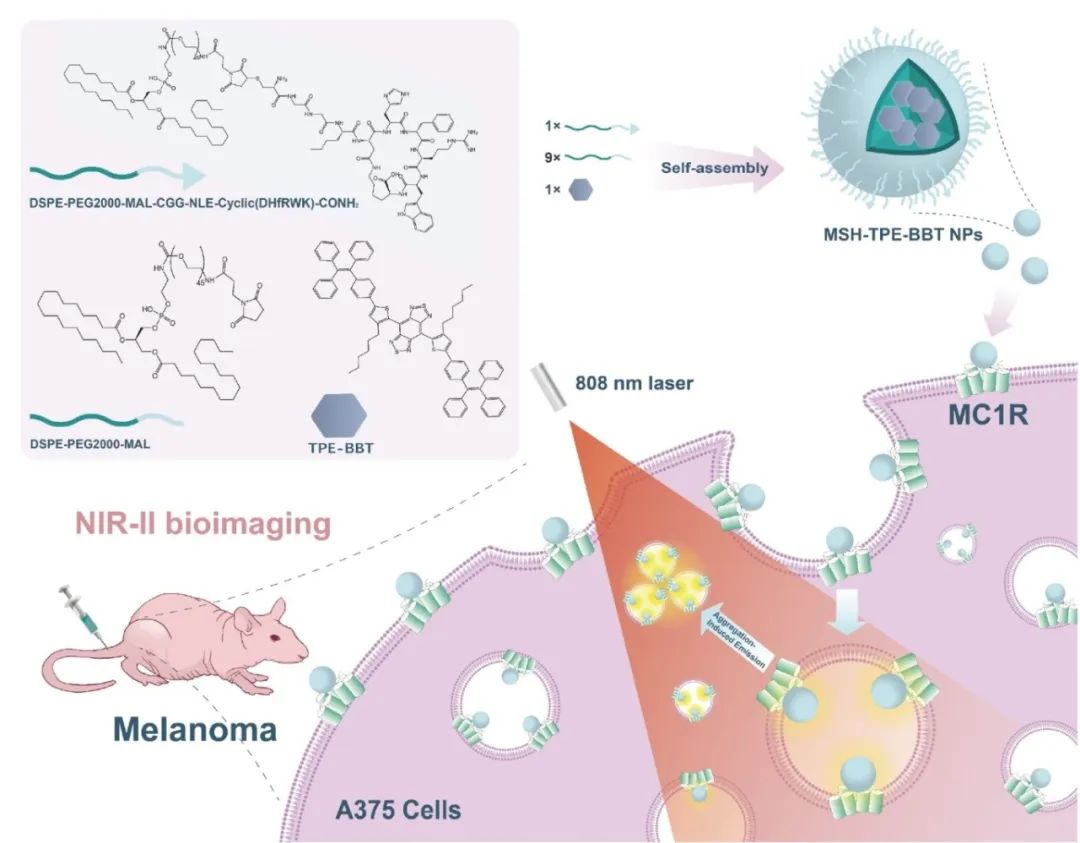 方案 1 MC1R 靶向的 MSH-TPE-BBT 纳米颗粒的制备以及在 808 nm激光照射下荷黑色素瘤小鼠的近红外二区(NIR-II)荧光成像流程。实验过程本次实验旨在制备一种新型的黑色素瘤靶向荧光探针,并对其性能进行全面评估,为黑色素瘤的早期诊断提供新的技术手段。(一)材料准备研究团队基于聚集诱导发光源(AIEgen)四苯乙烯 - 苯并双噻二唑(TPE - BBT)和靶向 MC1R 的 α - MSH 类似物(DSPEPEG2000 - MAL - CGG - NLE - Cycic (DHRWK)-CONH2 ),制备了名为 MSH - TPE - BBT NPs 的纳米颗粒。实验材料均为市售,TPE - BBT 按文献合成,其他材料如 DSPE - PEG2000 - MAL、MC1R 靶向肽等从相应公司购买。此外,还获取了多种细胞培养相关试剂以及不同细胞系,如人恶性黑色素瘤细胞(A375)、鼠乳腺癌细胞(4T1)、鼠黑色素瘤细胞(B16F10),实验动物选用 BALB/c 裸鼠 。(二)纳米颗粒的制备本次实验制备了两种纳米颗粒,分别是带有 MC1R 靶向肽的 MSH-TPE-BBT NPs,以及未添加靶向肽的 TPE-BBT NPs,具体步骤如下:1.准备原料溶液:将1mg(0.84μmol)的 TPE-BBT溶解于1mL 的四氢呋喃(THF)中;另取 9mg(3.11μmol)的 DSPE-PEG2000-MAL溶解于1mL THF中;再将1mg(0.24μmol)的 DSPEPEG2000 - MAL - CGG - NLE - Cycic (DHRWK)-CONH2溶解在适量的乙醇里。2.混合原料:将溶解好的DSPEPEG2000 - MAL - CGG - NLE - Cycic (DHRWK)-CONH2乙醇溶液,倒入含有 DSPE-PEG2000-MAL 的 THF 溶液中,充分搅拌混合均匀。3.超声处理:向上述两种溶液中加入去离子水,并使用功率为 150W 的超声波设备对溶液进行处理,处理时间设定为10 min。通过超声促使分子更好地分散和相互作用,从而形成稳定且分散均匀的纳米颗粒溶液。4.搅拌与过滤:将经过超声处理的溶液在室温环境下持续搅拌24 h,使反应充分进行。搅拌结束后,利用 0.22μm 的针头过滤器对溶液进行过滤操作,去除其中可能存在的未反应完全的大颗粒杂质等。5.储存备用:经过过滤得到的溶液,就是初步制备好的纳米颗粒溶液。在后续实验使用前,通过超滤的方法对溶液进行处理,调整其浓度到合适的水平。随后,将溶液放置在 4°C 的黑暗环境中储存,避免光照和温度变化对纳米颗粒的性质产生影响 。
方案 1 MC1R 靶向的 MSH-TPE-BBT 纳米颗粒的制备以及在 808 nm激光照射下荷黑色素瘤小鼠的近红外二区(NIR-II)荧光成像流程。实验过程本次实验旨在制备一种新型的黑色素瘤靶向荧光探针,并对其性能进行全面评估,为黑色素瘤的早期诊断提供新的技术手段。(一)材料准备研究团队基于聚集诱导发光源(AIEgen)四苯乙烯 - 苯并双噻二唑(TPE - BBT)和靶向 MC1R 的 α - MSH 类似物(DSPEPEG2000 - MAL - CGG - NLE - Cycic (DHRWK)-CONH2 ),制备了名为 MSH - TPE - BBT NPs 的纳米颗粒。实验材料均为市售,TPE - BBT 按文献合成,其他材料如 DSPE - PEG2000 - MAL、MC1R 靶向肽等从相应公司购买。此外,还获取了多种细胞培养相关试剂以及不同细胞系,如人恶性黑色素瘤细胞(A375)、鼠乳腺癌细胞(4T1)、鼠黑色素瘤细胞(B16F10),实验动物选用 BALB/c 裸鼠 。(二)纳米颗粒的制备本次实验制备了两种纳米颗粒,分别是带有 MC1R 靶向肽的 MSH-TPE-BBT NPs,以及未添加靶向肽的 TPE-BBT NPs,具体步骤如下:1.准备原料溶液:将1mg(0.84μmol)的 TPE-BBT溶解于1mL 的四氢呋喃(THF)中;另取 9mg(3.11μmol)的 DSPE-PEG2000-MAL溶解于1mL THF中;再将1mg(0.24μmol)的 DSPEPEG2000 - MAL - CGG - NLE - Cycic (DHRWK)-CONH2溶解在适量的乙醇里。2.混合原料:将溶解好的DSPEPEG2000 - MAL - CGG - NLE - Cycic (DHRWK)-CONH2乙醇溶液,倒入含有 DSPE-PEG2000-MAL 的 THF 溶液中,充分搅拌混合均匀。3.超声处理:向上述两种溶液中加入去离子水,并使用功率为 150W 的超声波设备对溶液进行处理,处理时间设定为10 min。通过超声促使分子更好地分散和相互作用,从而形成稳定且分散均匀的纳米颗粒溶液。4.搅拌与过滤:将经过超声处理的溶液在室温环境下持续搅拌24 h,使反应充分进行。搅拌结束后,利用 0.22μm 的针头过滤器对溶液进行过滤操作,去除其中可能存在的未反应完全的大颗粒杂质等。5.储存备用:经过过滤得到的溶液,就是初步制备好的纳米颗粒溶液。在后续实验使用前,通过超滤的方法对溶液进行处理,调整其浓度到合适的水平。随后,将溶液放置在 4°C 的黑暗环境中储存,避免光照和温度变化对纳米颗粒的性质产生影响 。
实验结果
(一)良好的材料特性

图 1 (a)TPE-BBT 在不同水分数(fw)的四氢呋喃(THF)/ 水混合液中的荧光发射光谱。(b)TPE-BBT 在 918nm 处的相对荧光强度(I/I₀)与 fw 的关系。I₀是 TPE-BBT 在 THF(fw = 0%)中的荧光发射强度。分子浓度:10⁻⁵mol/L;激发波长(λex) = 685nm。(c,d)(c)MSH-TPE-BBT 和(d)TPE-BBT 纳米颗粒的粒径和透射电镜(TEM)图像(插图)。标尺:100μm。(e - f)(e)MSH-TPE-BBT 纳米颗粒(λex = 685nm)、(f)TPE-BBT 纳米颗粒(λex = 685nm)和(g)吲哚菁绿(ICG,λex = 685nm)的吸收光谱和发射光谱。(h)水中五种不同浓度的 TPE-BBT 纳米颗粒以及在二氯乙烷(C₂H₄Cl₂)中的 IR26 在 850 至 1600nm 之间相应发射峰积分的吸光度拟合曲线。激发波长:808nm。(i)连续激光照射下,MSH-TPE-BBT 纳米颗粒(920nm 发射峰)、TPE-BBT 纳米颗粒(920nm 发射峰)和 ICG(810nm 发射峰)在各自相应发射峰处的相对荧光发射强度(I/I₀)。I₀:激光照射前的荧光峰强度;I:激光照射后的荧光峰强度。激发波长:808nm。(j)不同厚度鸡胸肉组织下 MSH-TPE-BBT 纳米颗粒、TPE-BBT 纳米颗粒和 ICG 的荧光图像。1:MSH-TPE-BBT 纳米颗粒;2:TPE-BBT 纳米颗粒;3:ICG。浓度:0.05mg/mL;激发波长:808nm;功率密度 = 0.7mW/cm²;1000nm 长通(LP)滤光片;曝光时间 = 100ms。(j 由睿光科技的NirVivo-Pro小动物活体成像系统拍摄)(k)MSH-TPE-BBT 纳米颗粒、TPE-BBT 纳米颗粒和 ICG 的荧光强度与穿透深度的拟合曲线。
通过1HNMR、MALDI - TOF - MS 和元素分析确认 TPE - BBT 成功合成。它在二氯甲烷中 500 - 850nm 有强吸收,750 - 1200nm 有强荧光发射,且具有聚集诱导发光特性。MSH - TPE - BBT NPs 和 TPE - BBT NPs 粒径分别为 122.12nm 和 133.55nm,呈均匀球形,带负电荷,MSH - TPE - BBT NPs 体系更稳定。二者在 685nm 有蕞大吸收,910nm 有荧光峰,在 NIR - II 区发射优于ICG。TPE - BBT NPs 量子产率达 31.6%,MSH - TPE - BBT NPs 和 TPE - BBT NPs 光稳定性强,远优于ICG,且组织穿透能力也比 ICG 更强。(二)低毒且靶向性好
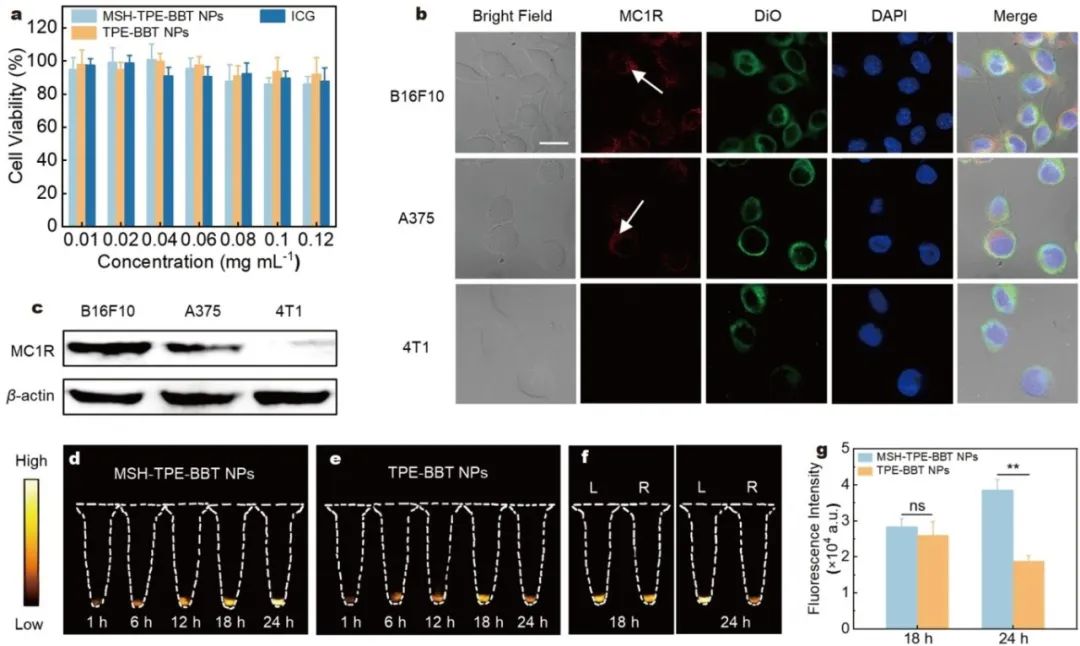
图 2 (a)用不同浓度的 MSH-TPE-BBT 纳米颗粒、TPE-BBT 纳米颗粒和 ICG 处理人黑色素瘤 A375 细胞 24h 后的细胞活力。(b)通过免疫细胞化学可观察到 MC1R 表达(红色)、细胞膜(用 DiO 标记,绿色)和细胞核(用 DAPI 标记,蓝色)。箭头分别指示 B16F10 细胞和 A375 细胞中 MC1R 的表达。比例尺:20μm。(c)通过蛋白质免疫印迹法检测 B16F10、A375 和 4T1 细胞中 MC1R 的表达。(d,e)(d)MSH-TPE-BBT 纳米颗粒或(e)TPE-BBT 纳米颗粒在 A375 细胞上孵育不同时间后产生的近红外二区(NIR-II)信号。(f)分别在 18h 和 24h 孵育后,A375 细胞与 MSH-TPE-BBT 纳米颗粒或 TPE-BBT 纳米颗粒孵育产生的 NIR-II 信号对比。L:MSH-TPE-BBT 纳米颗粒。R:TPE-BBT 纳米颗粒。(g)A375 细胞在与 MSH-TPE-BBT 纳米颗粒或 TPE-BBT 纳米颗粒孵育 18h 或 24h 后,NIR-II 信号的统计分析(ns 表示无显著性差异,** 表示 P < 0.01)。
CCK - 8 实验显示,在 0.01 - 0.12mg/mL 浓度范围内,MSH - TPE - BBT NPs 和 TPE - BBT NPs 对A375细胞毒性低,细胞存活率超 85%。免疫 ocytochemistry 和 Western blot 证实 A375 和 B16F10 细胞表达 MC1R,4T1 细胞不表达。细胞实验表明,MSH - TPE - BBT NPs 靶向性出色,24h 时其在 A375 细胞的荧光强度显著高于 TPE - BBT NPs。(三)体内成像效果佳
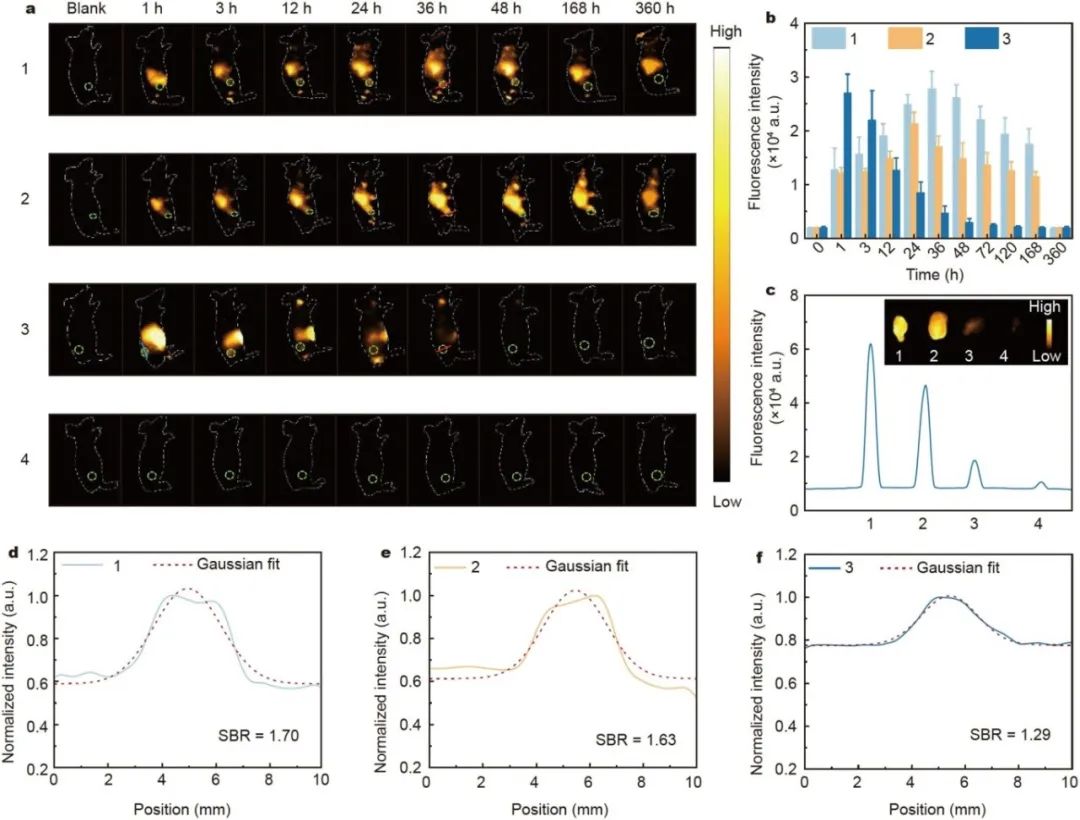
图 3(a)注射 MSH-TPE-BBT 纳米颗粒、TPE-BBT 纳米颗粒、ICG 或 PBS 后不同时间点小鼠的荧光图像。肿瘤以绿色圆圈表示。浓度:0.5mg/mL;激发波长(λex)=808nm;功率密度:0.7mW/cm²;1000nm 长通(LP)滤光片;曝光时间 = 30ms。(a 由睿光科技的NirVivo-Pro小动物活体成像系统拍摄)(b)各组肿瘤信号随时间变化的统计图。(c)注射后 36h 离体肿瘤的荧光信号和荧光成像(n=3)。曝光时间 = 100ms。(d-f)小鼠分别注射(d)MSH-TPE-BBT 纳米颗粒、(e)TPE-BBT 纳米颗粒和(f)ICG 36h 后,用红线标记的肿瘤的横截面荧光强度分布。线长:1cm。1:MSH-TPE-BBT 纳米颗粒;2:TPE-BBT 纳米颗粒;3:ICG;4:PBS。拍摄设别使用
给皮下黑色素瘤小鼠尾静脉注射 MSH - TPE - BBT NPs、TPE - BBT NPs 或 ICG 后,MSH - TPE - BBT NPs 在肿瘤的荧光信号 36h 达蕞强,且肿瘤滞留时间长、信号强,其肿瘤信号背景比(SBR)为 1.70,优于 TPE - BBT NPs 和 ICG。药代动力学研究发现,MSH - TPE - BBT NPs 和 TPE - BBT NPs 首先在肝脏和脾脏积累,MSH - TPE - BBT NPs 能逐渐到达并积累在肿瘤,而 ICG 在体内停留时间短、代谢快。血液生化指标和病理切片显示,MSH - TPE - BBT NPs 生物an全性良好。
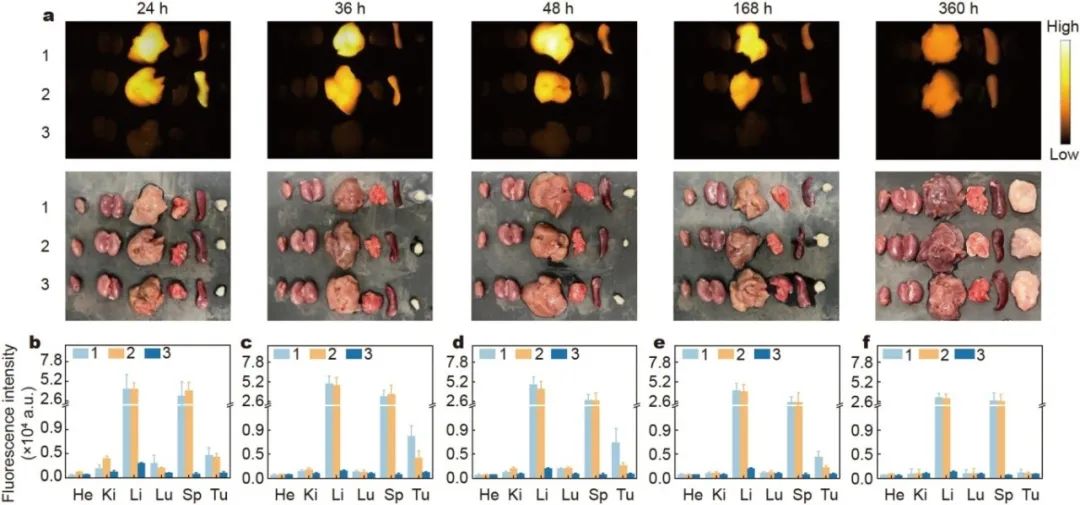
图 4 (a)尾静脉注射 MSH-TPE-BBT 纳米颗粒、TPE-BBT 纳米颗粒和 ICG 后不同时间点,它们在体内的生物分布的荧光图像和明场图像。激发波长(λex)为 808nm;功率密度为 0.7mW/cm²;使用 1000nm 长通(LP)滤光片;曝光时间为 6ms。(a 由睿光科技的NirVivo-Pro小动物活体成像系统拍摄)(b - f)分别在注射 MSH-TPE-BBT 纳米颗粒、TPE-BBT 纳米颗粒或 ICG 后(b)24 小时、(c)36 小时、(d)48 小时、(e)168 小时和(f)360 小时,小鼠主要器官和肿瘤的荧光强度统计。1:MSH-TPE-BBT 纳米颗粒;2:TPE-BBT 纳米颗粒;3:ICG。He:心脏;Ki:肾脏;Li:肝脏;Sp:脾脏;Tu:肿瘤。
研究意义
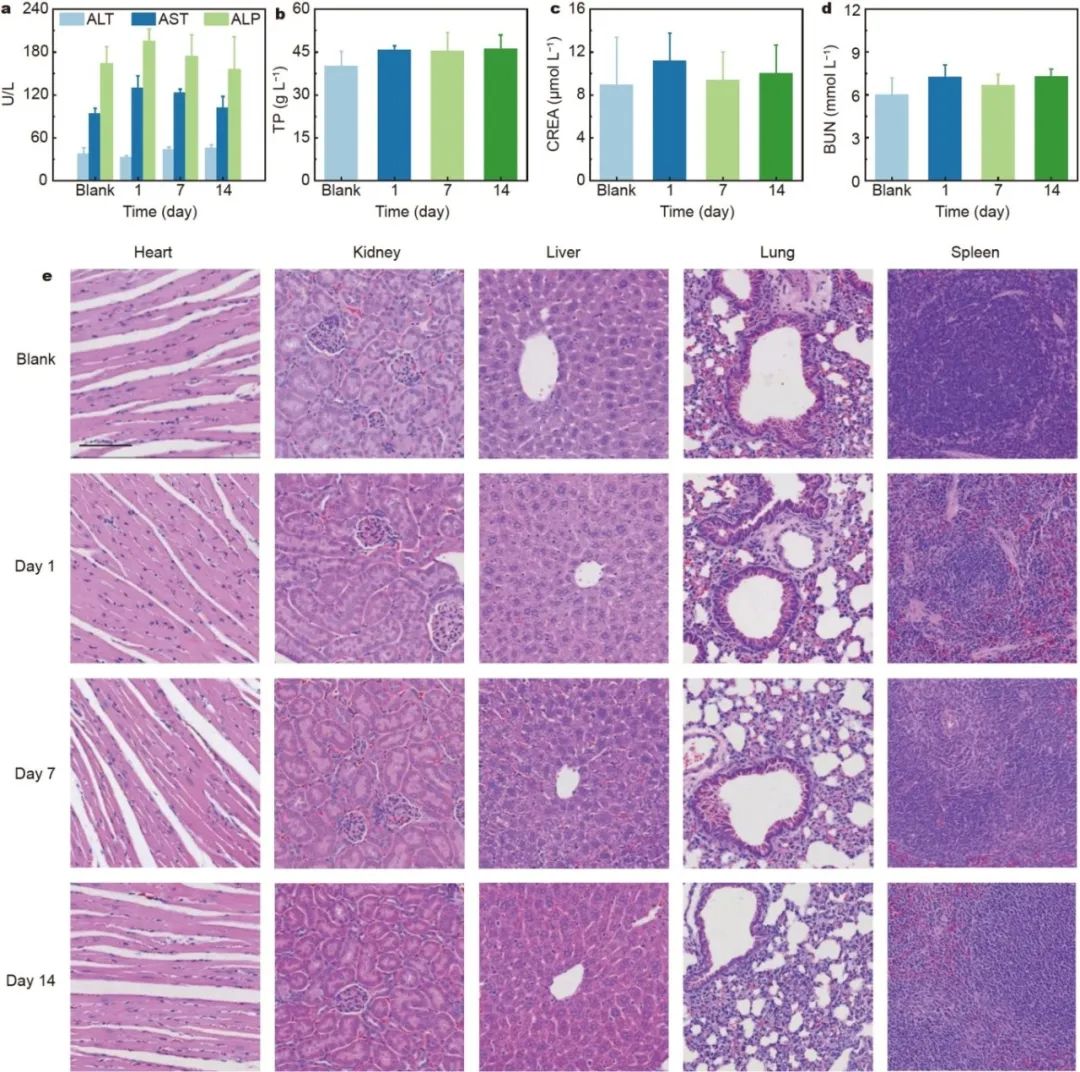
图 5(a - d)注射 MSH - TPE - BBT 纳米颗粒前以及注射后 1 天、7 天和 14 天的血清生化分析,(a)谷丙转氨酶(ALT)、谷草转氨酶(AST)、碱性磷酸酶(ALP);(b)总蛋白(TP);(c)肌酐(CREA);(d)尿素氮(BUN)(n = 3)。(e)健康小鼠在注射 MSH - TPE - BBT 纳米颗粒前以及注射后 1 天、7 天和 14 天主要器官的病理切片(n = 3)。比例尺 = 100μm。
这项研究成功开发的 MSH - TPE - BBT NPs 纳米颗粒,在黑色素瘤早期诊断方面展现出巨大潜力。其良好的组织穿透性、光稳定性、生物an全性和特异性靶向性,克服了传统诊断方法和现有荧光探针的诸多缺陷。未来,有望进一步推动黑色素瘤早期诊断技术的临床转化,提高黑色素瘤患者的早期诊断率和生存率,为皮肤癌的防治开辟新路径。

